小细胞肺癌(SCLC)是一种高度侵袭性的神经内分泌肿瘤,占所有肺癌病例的13%-15%。2025年,全球新发SCLC病例预计达28万例。SCLC具有增殖速度快、早期易发生远处转移、对放化疗敏感但极易复发耐药的特点,患者总体预后较差。既往数据显示,未经治疗的广泛期SCLC患者中位生存期仅12-15个月,即使接受规范治疗,广泛期SCLC患者5年生存率不足5%。总的来看,小细胞肺癌领域存在急迫的、未满足的临床需求。近年来,随着一批新靶点在小细胞肺癌领域持续突破,如DLL3、B7H3、SEZ6等,小细胞肺癌的治疗曙光已现。
DLL3是小细胞肺癌领域一颗冉冉升起的新星。DLL3(Delta‐like canonical Notch ligand 3)是一种高度肿瘤选择性的细胞表面标记物,由619个氨基酸组成。研究发现,DLL3在正常细胞中低表达,但在大约80%的小细胞肺癌(SCLC)和其他神经内分泌肿瘤(NEN)中高度表达。这种在健康细胞和癌细胞表面表达的差异性使DLL3成为一个极具潜力的肿瘤治疗靶点。
目前,靶向DLL3的药物研发包括多抗、ADC以及细胞治疗药物。首款DLL3/CD3双抗tarlatamab已获批上市,验证了靶点的成药性。再鼎医药/宜联生物的ZL-1310、勃林格殷格翰的BI 764532、泽璟制药的ZG006处于临床Ⅲ期。
表:靶向DLL3药物在研格局
数据来源:公开数据整理

表:Tarlatamab的Ⅲ期DeLLphi-304研究mOS数据
数据来源:安进官网
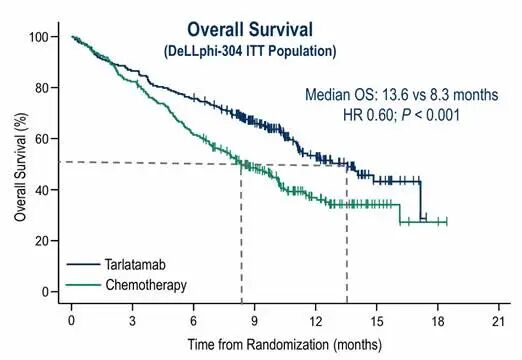
图:ZG006分子结构
数据来源:泽璟制药宣传资料
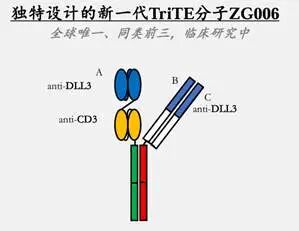
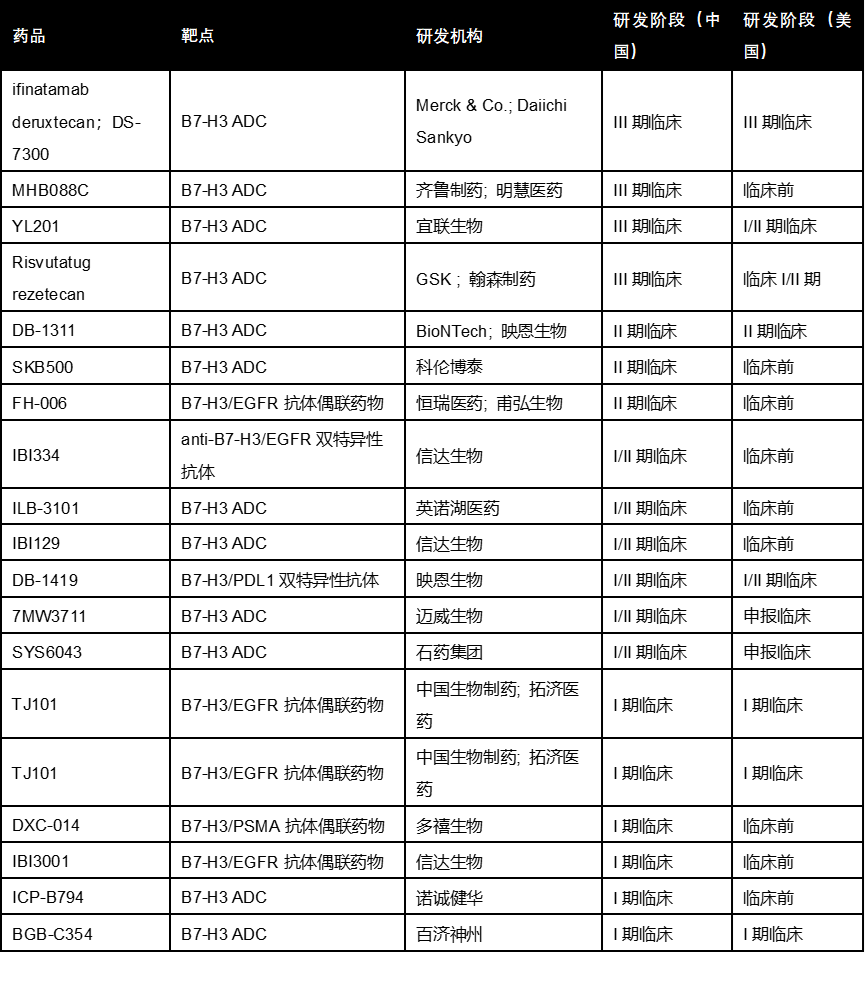
表:靶向B7H3药物在研格局
数据来源:公开数据整理
(1)DS-7300是一款由第一三共和默沙东合作开发的B7-H3 ADC,目前处于临床Ⅲ期,近期遭遇安全性问题研发被暂停。
在一项名为IDeate-Lung01的Ⅱ期研究中,DS-7300在在经治的广泛期小细胞肺癌(ES-SCLC)患者中展现出卓越的疗效。研究共纳入88例ES-SCLC患者,其中I-DXd 8 mg/kg组纳入46例患者,12mg/kg组纳入42例患者。研究结果显示,12mg/kg组和8mg/kg组经BICR确认的ORR分别为54.8%和26.1%,12mg/kg和8mg/kg剂量组的中位PFS分别为5.5个月和4.2个月,中位OS分别为11.8个月和9.4个月。
尽管DS-7300 二期疗效显著,但转折出现在三期临床试验中。2025年12月,第一三共宣布,由于DS-7300的三期研究(IDeate-Lung02)中五级间质性肺炎(ILD)发生率比预期更高,因此该临床试验暂停。未来,DS-7300何去何从,仍有待关注。
(2)尽管全球领先的B7H3 ADC研发受阻,但MNC依然对这一靶点高度关注。近年来,四款国产B7H3 ADC相继授权,涉及企业包括翰森制药、映恩生物、宜联生物和英诺湖医药。2026年初,两款国产B7H3 ADC对外授权,分别是宜联生物的YL201授权罗氏,英诺湖医药的ILB-3101授权Ellipses Pharma。不难发现,即使在第一三共/默沙东的DS-7300研发受阻后,罗氏等企业仍然前赴后继,凸显B7H3 ADC药物的价值。
表:国产B7H3 ADC授权(亿美元)
数据来源:公开数据整理

表:靶向SEZ6药物在研格局
数据来源:公开数据整理

ABBV-706是一种靶向SEZ6的抗体偶联药物(ADC),有效载荷为TOP1i,目前处于临床Ⅱ期。ABBV-706的Ⅰ期研究纳入年龄≥18岁、经组织学或细胞学证实为广泛期SCLC(ES-SCLC)、接受过至少1线含铂化疗的患者。患者按1:1随机分配接受ABBV-706 1.8 mg/kg或2.5 mg/kg静脉注射,每3周一次,21天为一个周期。研究结果显示,在总人群(n = 80)中,确认的客观缓解率(cORR)为58%,总人群中位无进展生存期(PFS)为5.7个月。
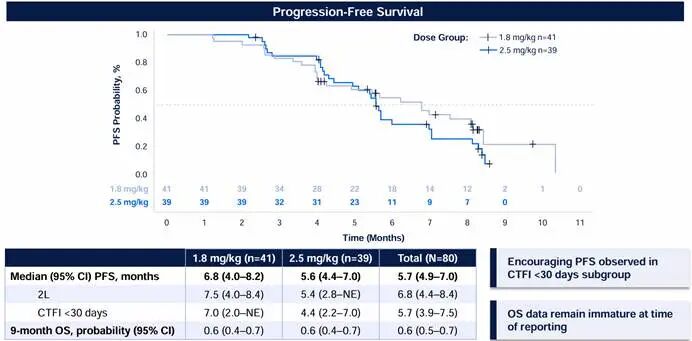
亚族数据显示,接受过2线既往治疗(n = 30)或至少3线既往治疗(n = 50)的患者,cORR分别为77%和46%。此外,接受1.8 mg/kg剂量治疗的患者(n = 41)中,cORR为56%,mPFS为6.8m;接受2.5 mg/kg剂量治疗的患者(n = 39)中,cORR为59%,mPFS为5.6m。
安全性方面,在总人群中,90%的患者报告了任何级别的治疗相关不良事件(TRAEs),3级及以上TRAEs为63%。接受1.8 mg/kg剂量治疗的患者G3 TRAE为49%;接受2.5 mg/kg剂量治疗的患者G3 TRAE为77%。
图:ABBV-706的mPFS数据
数据来源:2025ESMO
近年来,小细胞肺癌领域新兴靶点不断涌现,如DLL3、B7H3和SEZ6等。首款CD3/DLL3双抗Tarlatamab于2024年上市,2025年斩获6.27亿美元的优异商业化成绩;国内泽璟制药的CD3/DLL3/DLL3三抗和再鼎医药的DLL3 ADC临床数据优异,有望超越Tarlatamab后来居上。首款B7H3 ADC药物因安全性研发暂停,但一批国产B7H3 ADC成功授权MNC,如瀚森制药的HS-20093授权GSK、宜联生物的YL201授权罗氏,有望诞生兼具疗效和安全性的品种。目前仅一款SEZ6 ADC处于临床阶段,为艾伯维的ABBV-706,但艾伯维的野心远不止ABBV-706,通过引进泽璟制药的ZG006,艾伯维有望进一步探索SEZ6 ADC联合CD3/DLL3/DLL3的潜力,发挥1+1>2的优势。期待小细胞肺癌领域更多优异的创新药诞生。
版权声明:本文转自药事纵横,如不希望被转载的媒体或个人可与我们联系,我们将立即删除
Feel free to call us on
025-85998075
Drop us a line anytime at
sales@popebiotech.com,
and we’ll get back
soon.
Come visit us at 南京市江宁区科学园乾德路5号