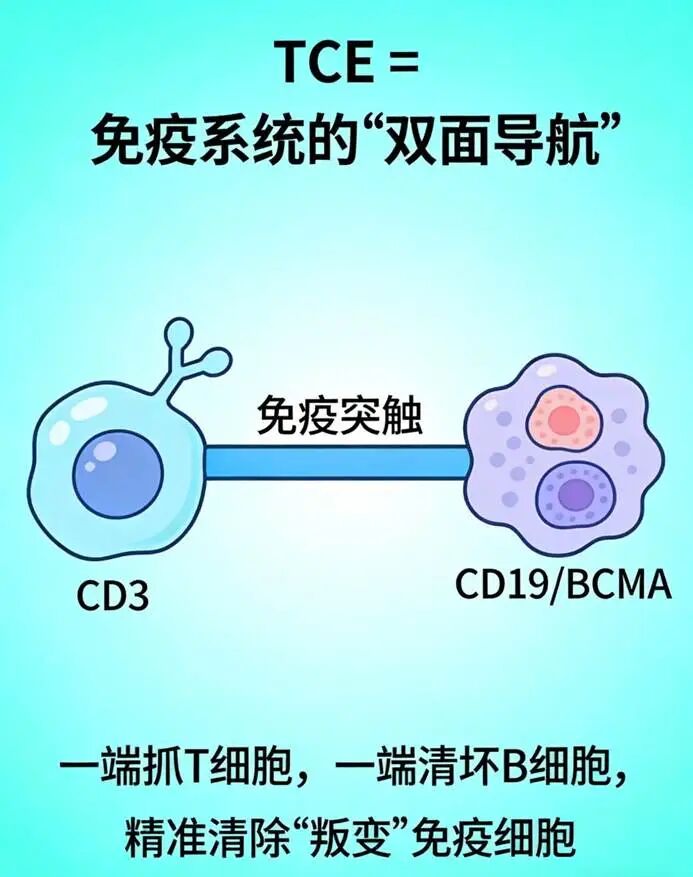
在肿瘤免疫治疗的浩瀚星图中,T细胞衔接器(T-cell Engager, TCE)正以其独特的“双靶向”机制冉冉升起,成为继免疫检查点抑制剂和CAR-T疗法之后的第三座里程碑。不同于需要体外复杂制备的CAR-T细胞疗法,也不同于依赖预存浸润淋巴细胞的PD-1/PD-L1抑制剂,TCE药物宛如一位精妙的“分子桥梁工程师”,能够直接在体内将患者自身的T细胞“牵引”至肿瘤细胞或病理细胞身旁,强行构建“免疫突触”,从而激活内源性T细胞的杀伤潜能。从2014年首个TCE药物贝林妥欧单抗获批用于复发/难治性B细胞急性淋巴细胞白血病(R/R B-ALL),到2024年Tarlatamab打破实体瘤治疗僵局获批用于小细胞肺癌,再到自身免疫疾病领域展现出的“免疫重置”潜力,TCE技术正在经历从血液肿瘤向实体瘤、从恶性疾病向自身免疫性疾病的双重跨越。然而,这一历程并非坦途,抗原脱靶毒性、细胞因子释放综合征(CRS)以及实体瘤免疫抑制微环境等挑战依然严峻。本文将基于最新研究进展,科学客观地剖析TCE的作用机制、技术演进、临床突破及未来挑战,探讨这一“可编程免疫调节工具”如何突破现有治疗边界。
一、TCE核心机制:构建“免疫突触”的精准导航系统
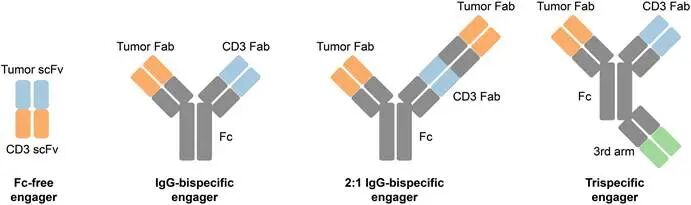
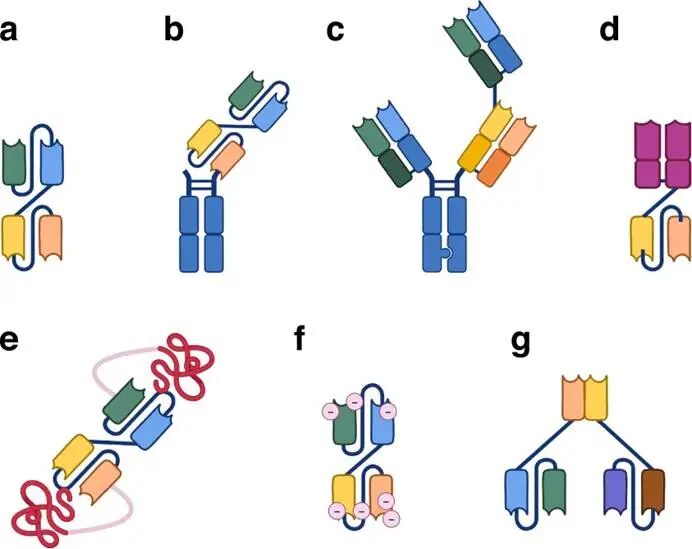
TCE药物的核心逻辑在于打破免疫耐受,通过双特异性抗体结构同时结合T细胞表面的CD3复合物和靶细胞表面的特异性抗原。这种“双向衔接”机制绕过了T细胞天然依赖MHC分子呈递抗原的限制,直接将静息态T细胞招募至靶细胞周围(距离<40 nm),形成稳定的“免疫突触”。在这一微观结构中,TCE的CD3结合域识别T细胞受体(TCR)复合物中的CD3ε链,触发磷酸化级联反应,启动T细胞活化信号;而肿瘤抗原结合域则像锚点一样将TCE固定在靶细胞表面。一旦免疫突触形成,活化的T细胞随即释放穿孔素和颗粒酶,直接裂解靶细胞,同时分泌干扰素-γ(IFN-γ)、肿瘤坏死因子-α(TNF-α)等细胞因子,放大局部免疫应答。这种机制不仅适用于高增殖活性的肿瘤细胞,对静止期细胞同样有效,且不依赖于抗体Fc段的ADCC效应,展现了其独特的杀伤广度。CD3分子作为T细胞激活的“信号枢纽”,其胞内结构域包含免疫受体酪氨酸激活基序(ITAM),是信号转导的关键开关。绝大多数TCE药物选择靶向CD3,正是基于其在T细胞激活信号通路中的核心地位。通过工程化设计,TCE能够以可控的方式“ hijack”这一信号通路,将原本对肿瘤“视而不见”的T细胞重新编程为高效的杀伤机器。图1.双特异性及多特异性免疫细胞衔接器分子结构的示意图
二、技术演进:从“1+1”到“多特异性”的结构革命
TCE药物的设计迭代始终围绕“提升精准性、降低毒性”这一核心目标展开,其分子结构经历了从简单到复杂、从单一到多维的深刻变革。
2.1 “1+1”双特异性格式:奠基之作
早期的TCE药物如贝林妥欧单抗采用经典的“1+1”结构,即一个肿瘤抗原结合臂(如抗CD19 scFv)和一个T细胞结合臂(抗CD3 scFv)通过柔性连接肽相连。这种双单链可变片段(BiTE)结构分子量小(约55 kDa),穿透力强,甚至能透过血脑屏障,但半衰期极短(约2小时),需持续静脉输注给药。此外,单一的抗原结合臂可能导致对低抗原密度正常组织的误伤,且易因肿瘤抗原丢失而产生耐药。
2.2 “2+1”非对称结构:提升肿瘤选择性
为解决特异性不足的问题,“2+1”格式应运而生。该结构包含两个肿瘤抗原结合臂和一个CD3结合臂,典型代表为Glofitamab(CD20×CD3)。其设计巧妙之处在于利用亲和力效应:当靶细胞表面抗原密度高时,两个TAA结合臂可同时结合,形成高亲和力相互作用,牢固锁定T细胞;而正常细胞因抗原密度低,难以同时满足两个结合臂的结合需求,从而大幅降低脱靶毒性。这种“双钩”设计显著提升了治疗窗口,使Glofitamab在复发/难治性弥漫大B细胞淋巴瘤(DLBCL)中取得了80.8%的客观缓解率(ORR)。图2.TCE的迭代设计结构示意图
2.3 “1+1+1”三特异性格式:应对复杂性与耐药性
面对肿瘤异质性和免疫抑制微环境,三特异性TCE进一步升级。这类分子可同时靶向CD3、两个不同的肿瘤抗原(如BCMA和CD38),或一个肿瘤抗原加一个T细胞共刺激分子(如CD28、4-1BB)。前者能有效防止因单一抗原丢失导致的免疫逃逸,后者则通过提供共刺激信号,增强T细胞在免疫抑制环境中的存活与功能,特别适用于实体瘤治疗。例如,针对多发性骨髓瘤的ISB 2001同时靶向BCMA和CD38,展现了深度缓解潜力。
2.4条件激活与前药设计:智能开关的引入
为了进一步降低全身毒性,新一代TCE引入了“智能开关”机制。包括蛋白酶激活型(如CX-904,仅在肿瘤微环境中被特定蛋白酶切割激活)、pH敏感型(在酸性肿瘤微环境中解除掩蔽)以及Pro-XTEN掩蔽技术(如AMX-818,利用延伸多肽遮蔽CD3结合域,直至被肿瘤相关蛋白酶切割)。这些设计使得TCE在血液循环中保持“休眠”状态,仅在到达肿瘤部位后才被激活,治疗窗口可扩大数十倍甚至上百倍。
2.5靶向胞内抗原:突破“不可成药”壁垒
传统TCE仅能识别细胞表面抗原,而新一代TCR样TCE(如Tebentafusp)通过模拟T细胞受体,识别由HLA分子呈递的胞内抗原肽段。这一突破将靶点范围扩展至KRAS突变、p53突变等曾经“不可成药”的胞内驱动基因,为葡萄膜黑色素瘤等难治性肿瘤带来了曙光。
三、临床突破:从血液肿瘤到实体瘤的跨越
3.1血液肿瘤:确立标准治疗地位
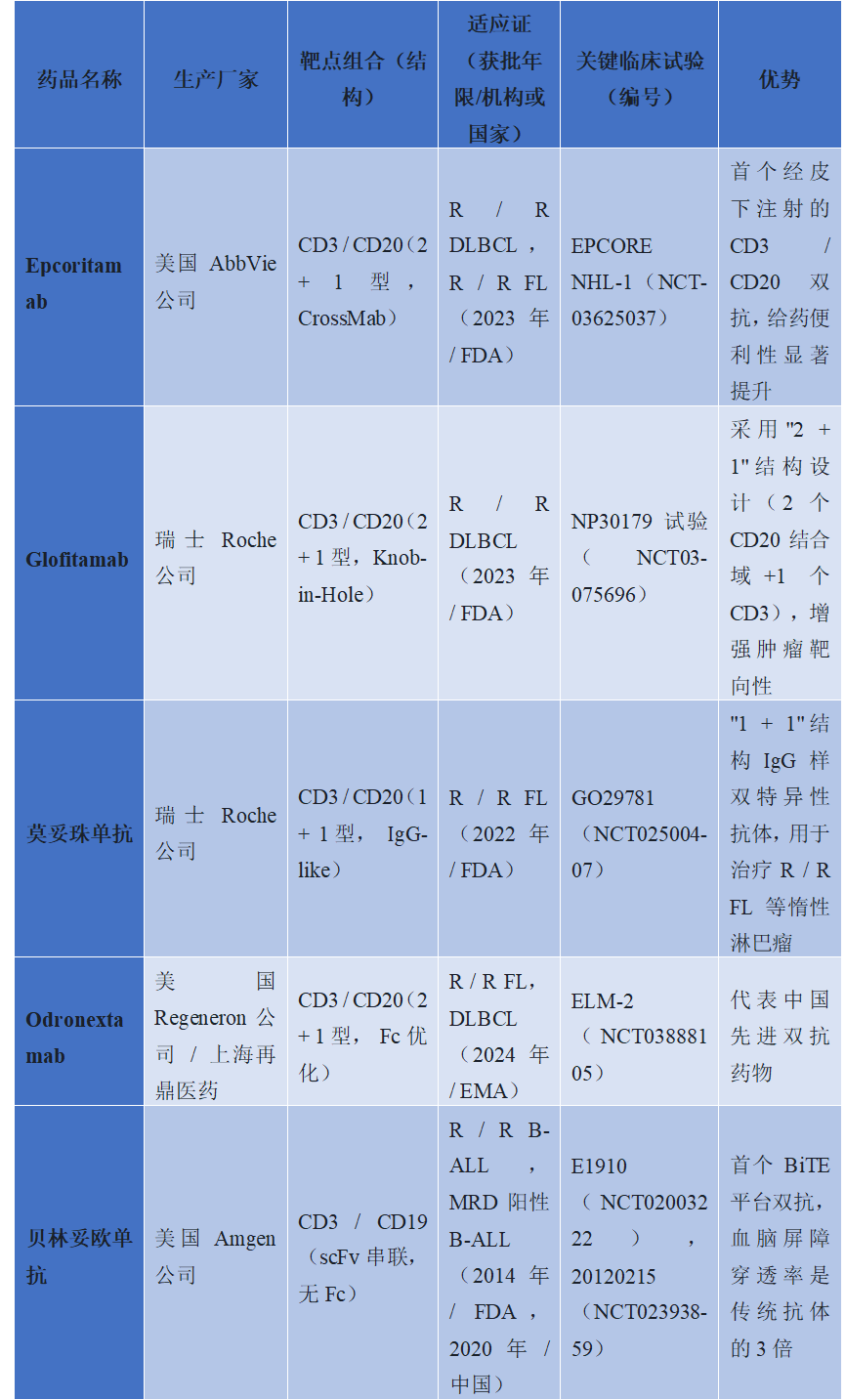
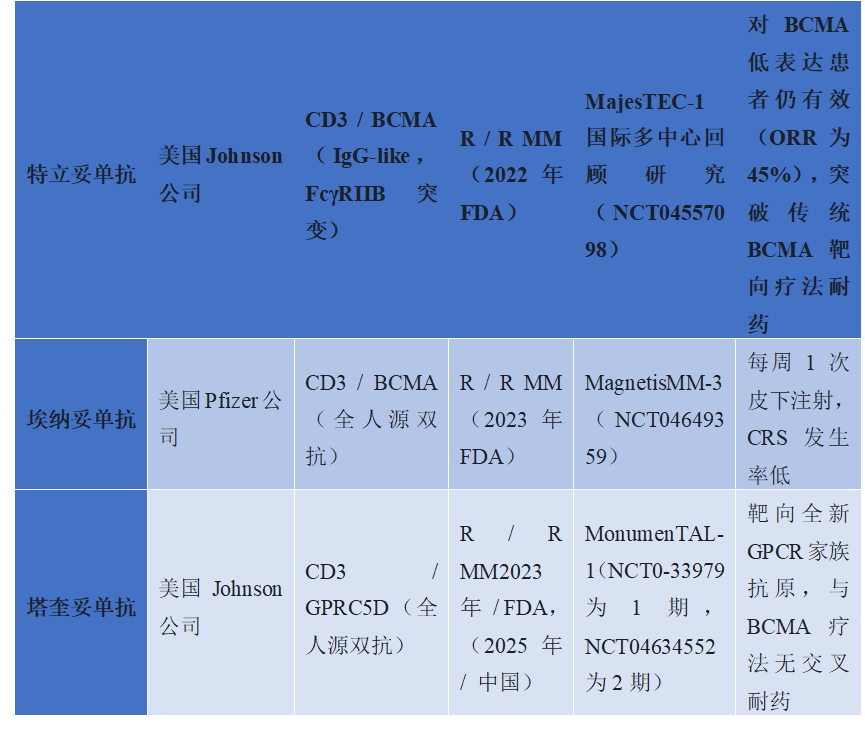
在血液肿瘤领域,TCE已展现出颠覆性的疗效。贝林妥欧单抗作为先行者,显著提高了R/R B-ALL患者的生存率,儿童患者5年总生存期可达78.4%。针对多发性骨髓瘤,特立妥单抗(BCMA×CD3)和塔奎妥单抗(GPRC5D×CD3)相继获批,为复发难治患者提供了新的希望,ORR分别达到67%和74%。CD20靶向的Epcoritamab、Glofitamab和莫妥珠单抗也在DLBCL和滤泡性淋巴瘤(FL)中取得了优异数据,其中莫妥珠单抗凭借较低的CRS发生率(39%)和持久的缓解时间(中位DOR达46.4个月),成为惰性淋巴瘤治疗的重要选项。
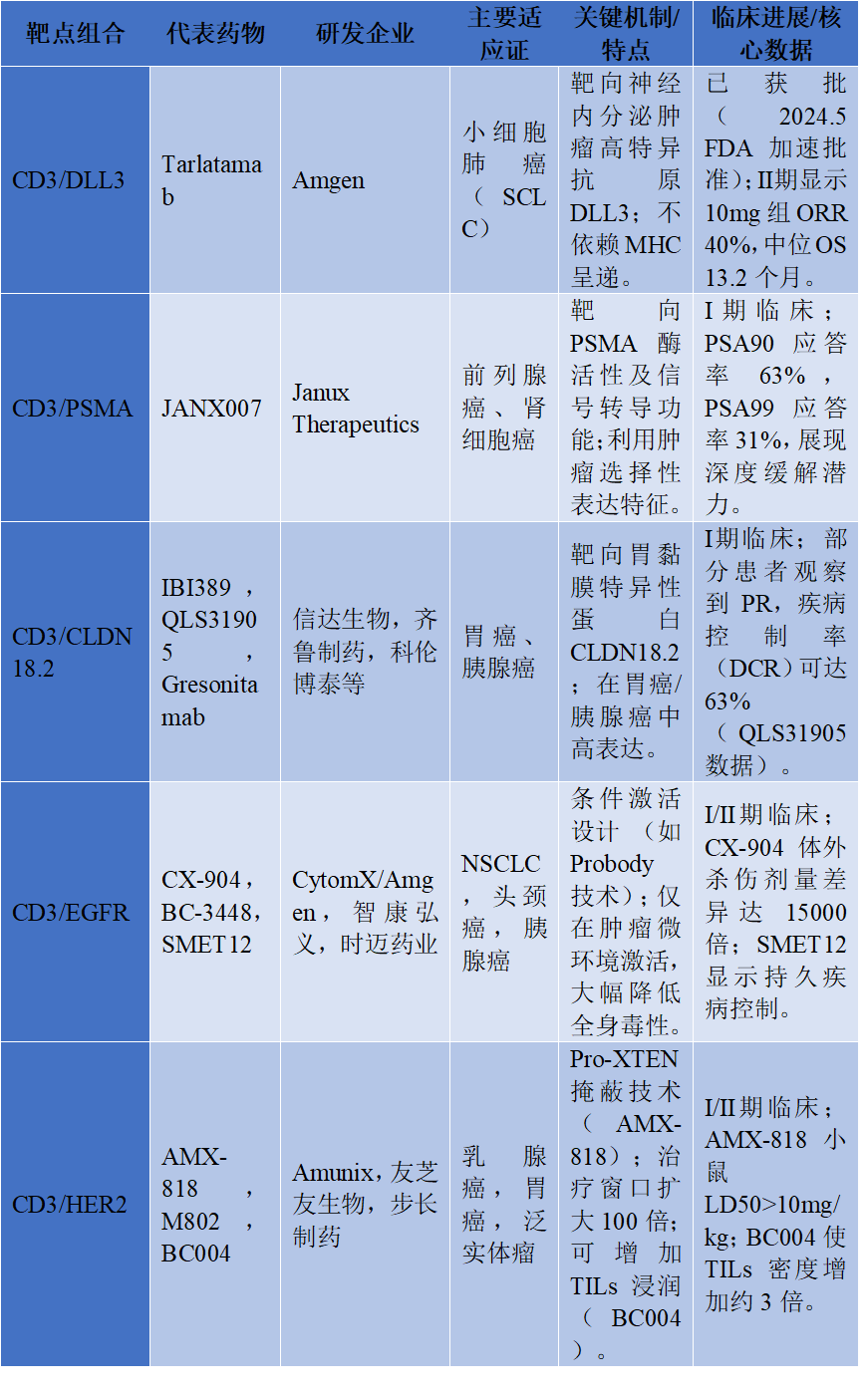
3.2实体瘤:破冰之旅正式开启
实体瘤曾是TCE治疗的“禁区”,主要受制于抗原脱靶毒性和免疫抑制微环境。然而,随着高特异性靶点的发现和技术改良,这一局面正在改变。2024年5月,Tarlatamab(CD3/DLL3)获FDA加速批准,成为首个用于治疗广泛期小细胞肺癌(ES-SCLC)的TCE药物。DLL3在85%的SCLC中高表达,而在正常组织中表达极低,赋予了Tarlatamab极高的治疗指数。Ⅱ期临床数据显示,10mg剂量组ORR达40%,中位OS达13.2个月,显著优于历史对照。此外,针对胃癌和胰腺癌的CLDN18.2靶向TCE(如QLS31905、IBI389)、针对前列腺癌的PSMA靶向TCE(如JANX007)、以及针对EGFR突变型肺癌的条件激活TCE(如CX-904、BC-3448)均处于临床试验阶段,并初步显示出抗肿瘤活性。特别是JANX007在晚期前列腺癌中实现了63%的患者PSA下降≥90%,展现了深度缓解潜力。
3.3自身免疫疾病:开启“免疫重置”新范式
TCE的应用边界正迅速拓展至自身免疫疾病领域。传统B细胞耗竭疗法(如利妥昔单抗)无法清除长寿命浆细胞,导致疾病复发。而TCE通过精准靶向不同B细胞亚群,有望实现更彻底的“免疫重置”。CD3/CD19双抗可清除B细胞及前浆细胞,从源头抑制自身抗体生成;CD3/BCMA双抗则直接靶向产生致病性抗体的浆细胞。初步临床探索显示,贝林妥欧单抗在难治性类风湿关节炎中实现了深度B细胞耗竭且未引发严重CRS,Teclistamab在重症系统性红斑狼疮(SLE)中也展现了协同清除效应。尽管部分早期数据存在波动,但其独特的机制优势仍使其成为极具潜力的治疗策略。
四、挑战与创新:破解治疗瓶颈的关键路径
尽管前景广阔,TCE药物的临床转化仍面临三大核心挑战:
4.1CRS与神经毒性
TCE强力激活T细胞往往伴随大量细胞因子释放,引发CRS,严重时可能导致多器官功能障碍。此外,部分药物(如贝林妥欧单抗)可能引起免疫效应细胞相关神经毒性综合征(ICANS)。解决策略包括:优化CD3结合域亲和力,采用“阶梯式”给药方案,开发条件激活型TCE,以及联合使用IL-6受体拮抗剂(如托珠单抗)进行预防和管理。
4.2实体瘤微环境的免疫抑制
实体瘤中缺乏T细胞浸润、富含抑制性细胞(Tregs、MDSCs)及抑制性因子(TGF-β、IL-10),构成了TCE发挥作用的巨大障碍。未来策略包括:联合免疫检查点抑制剂(如PD-1抗体)解除T细胞耗竭;联用溶瘤病毒破坏细胞外基质促进T细胞浸润;靶向肿瘤相关成纤维细胞(CAFs)减少抑制因子分泌;以及开发能分泌细胞因子的TCE变体,就地重塑免疫微环境。
4.3抗原异质性与脱靶毒性
肿瘤抗原表达的异质性可能导致治疗失败,而正常组织低水平表达靶抗原则可能引发脱靶毒性。应对之道在于开发多特异性TCE以覆盖多个抗原表位,利用AI辅助设计优化抗原结合域的特异性,以及采用前述的条件激活技术确保药物仅在肿瘤部位生效。
五、结语
总的来说,TCE代表了肿瘤免疫治疗乃至自身免疫疾病治疗的一次范式转移。它无需复杂的体外细胞制备,成本相对低廉,且具有“即用型”和模块化设计的优势,能够快速响应不同疾病的临床需求。从血液肿瘤的广泛应用,到实体瘤的破冰突围,再到自身免疫病的潜在颠覆,TCE正逐步证明其作为“通用型免疫治疗平台”的价值。当然,前路依然充满挑战。CRS的管理、实体瘤微环境的攻克、以及长期安全性的验证,都需要科研人员持续的创新与探索。随着多特异性分子、条件激活技术、人工智能辅助设计等前沿手段的深度融合,我们有理由相信,新一代TCE药物将更加精准、安全、高效。未来,TCE或许不再仅仅是抗肿瘤武器,更将成为一种可编程的免疫调节工具,在更广泛的疾病谱系中重塑健康的防线,开启免疫治疗的新纪元。[1] Phillips TJ, Carlo-Stella C, Morschhauser F, et al. Glofitamab in Relapsed/Refractory Mantle Cell Lymphoma: Results From a Phase I/II Study. J Clin Oncol. 2025 Jan 20;43(3):318-328. doi: 10.1200/JCO.23.02470.[2] Muth A, Holzem A, Neumann AS, et al. T cell exhaustion in bi- and trispecific T cell engager therapy in hematologic malignancies: Mechanisms and implications. Med. 2026 Feb 27:101031. doi: 10.1016/j.medj.2026.101031.[3] Xue E, Deng X, Doffe F, et al. Trial Watch - bispecific T cell engagers and higher-order multispecific immunotherapeutics. Oncoimmunology. 2026 Dec 31;15(1):2632421. doi: 10.1080/2162402X.2026.2632421.[4] Albayrak G, Wan PK, Fisher K, et al. T cell engagers: expanding horizons in oncology and beyond. Br J Cancer. 2025 Nov;133(9):1241-1249. doi: 10.1038/s41416-025-03125-y.
版权声明:本文转自药事纵横,如不希望被转载的媒体或个人可与我们联系,我们将立即删除