近日,第一三共宣布,已在一项首次用于评估DS3610治疗晚期、转移性或不可切除实体瘤患者的1期试验中完成首位患者给药,DS3610是一款STING激动剂ISAC药物。

这也是继Mersana的XMT-2056和Takeda(武田)的Plozalizumab plevistinag折戟后的又一款ADC药物进入临床试验中。
这项多中心、开放标签、首次用于人体的1期临床试验将评估DS3610在患有晚期、转移性或无法切除的实体瘤且无其他标准治疗方案可用的患者中的安全性、耐受性、初步疗效和药代动力学。剂量递增试验将评估逐渐增加DS3610剂量的安全性和耐受性,以确定在患有晚期、转移性或无法切除的实体瘤患者中进行扩展研究的推荐剂量。
该试验将评估安全性终点,包括剂量限制性毒性及不良事件。同时还将评估药代动力学和免疫原性终点,以及探索性疗效终点,包括客观缓解率、疾病控制率、缓解持续时间、起效时间、无进展生存期和总生存期。该试验预计将在全球多个地区招募患者,包括亚洲、欧洲和北美。
关于DS3610
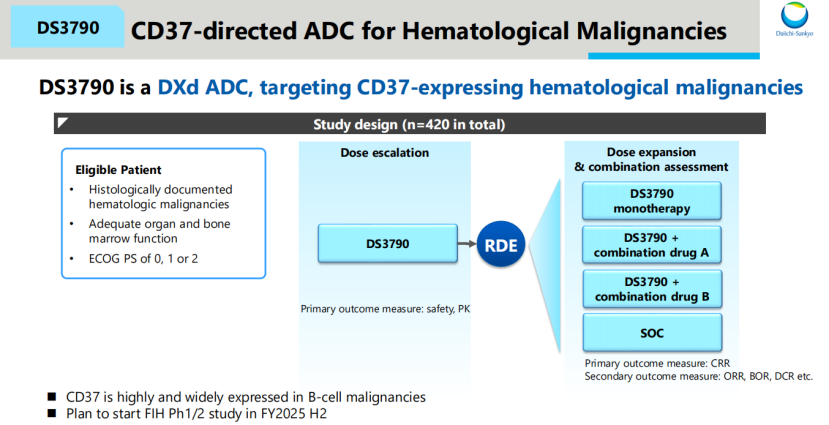
DS3610 是一种正在研究中的STING激动剂抗体药物偶联物(ADC),由具有新型Fc修饰的单克隆抗体与一种作为干扰素基因刺激因子(STING)激动剂的免疫调节有效载荷连接而成。DS3610 可将STING激动剂有效载荷直接递送至肿瘤微环境,激活人体免疫系统以靶向攻击癌细胞。
这一设计理念与 Mersana 的 XMT-2056 形成鲜明对比,后者保留了 FcγR 结合功能,从而实现双重递送,靶向肿瘤细胞和肿瘤驻留髓样细胞(例如树突状细胞、巨噬细胞)进行免疫重编程。
第一三共的ADC产品线由八种处于临床开发阶段的ADC组成,这些ADC均基于第一三共自主研发的ADC技术打造。
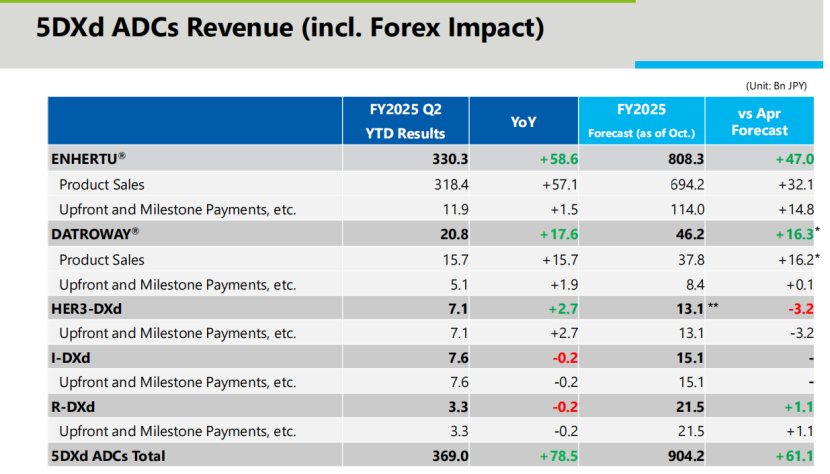
根据公司财报,其中,第一三共的ADC明星产品Enhertu(德曲妥珠单抗)在2025财年前2季度全球销售额为3184亿日元(约20.67亿美元),同比增长21.9%;公司预计Enhertu在2025年实现总营收8083亿日元(含版税约为52.48美元),同比增长6%。
参考资料:
公司官网
Feel free to call us on
025-85998075
Drop us a line anytime at
sales@popebiotech.com,
and we’ll get back
soon.
Come visit us at 2 Qiande Road, Life Science High Tech Zone, Jiang Ning District, Nanjing, Jiangsu Province, China